Что такое гниение
Суть в том, что сложнейшая по своему составу материя распадается на более простые элементы. Современное представление ученых об этом процессе, превращающем органические соединения в неорганические, можно описать следующими действиями:
- Бактерии гниения обладают метаболизмом, что разрывает химическим путем связи молекул органики, содержащих азот. Процесс питания происходит в форме захвата молекул белка и аминокислот.
- Ферменты, что выработаны микроорганизмами, в процессе расщепления высвобождают аммиак, амины, сероводород из молекул белка.
- Продукты, поступающие в организм бактерии гниения, используются для получения энергии.
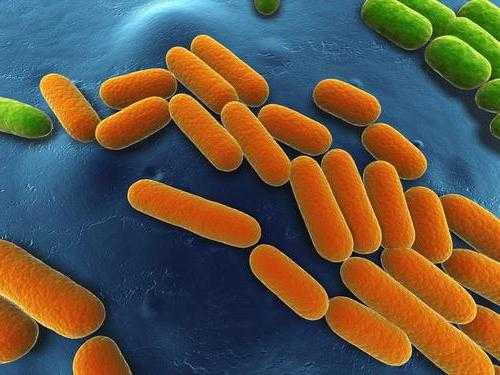
Физиологическое действие
Аммиак токсичен. По физиологическому действию на организм относится к группе веществ удушающего и нейротропного действия, способных при ингаляционном поражении вызвать токсический отёк лёгких и тяжёлое поражение нервной системы. Аммиак обладает как местным, так и резорбтивным действием.
Пары аммиака сильно раздражают слизистые оболочки глаз и органов дыхания, а также кожные покровы. Это человек и воспринимает как резкий запах. Пары аммиака вызывают обильное слезотечение, боль в глазах, химический ожог конъюнктивы и роговицы, потерю зрения, приступы кашля, покраснение и зуд кожи. При соприкосновении сжиженного аммиака и его растворов с кожей возникает жжение, возможен химический ожог с пузырями, изъязвлениями. Кроме того, сжиженный аммиак при испарении поглощает тепло, и при соприкосновении с кожей возникает обморожение различной степени. Запах аммиака ощущается при концентрации 37 мг/м³.
Предельно допустимая концентрация в воздухе рабочей зоны производственного помещения (ПДКр.з.) составляет 20 мг/м³. В атмосферном воздухе населённых пунктов и в жилых помещениях среднесуточная концентрация аммиака (ПДКс.с.) не должна превышать 0,04 мг/м³. Максимальная разовая концентрация в атмосфере — 0,2 мг/м³. Таким образом, ощущение запаха аммиака свидетельствует о превышении допустимых норм.
Раздражение зева проявляется при содержании аммиака в воздухе 280 мг/м³, глаз — 490 мг/м³. При действии в очень высоких концентрациях аммиак вызывает поражение кожи: 7—14 г/м³ — эритематозный, 21 г/м³ и более — буллёзный дерматит. Токсический отёк лёгких развивается при воздействии аммиака в течение часа с концентрацией 1,5 г/м³. Кратковременное воздействие аммиака в концентрации 3,5 г/м³ и более быстро приводит к развитию общетоксических эффектов.
В мире максимальная концентрация аммиака в атмосфере (больше 1 мг/м³) наблюдается на Индо-Гангской равнине, в Центральной долине США и в Туркестанской (ранее — Южно-Казахстанской) области Казахстана.
Денитрификация
В отличие от нитрификации и аммонификации, денитрификация является восстановительным процессом, а не окислительным, и он связан с возвращением азота в атмосферу. На такое способны как бактерии-прокариоты (и археи-прокариоты), так и эукариотами, а именно: грибами (в том числе дрожжевыми) и клетками печени животных.

Денитрификация осуществляется в анаэробных условиях, поскольку подавляется молекулами кислорода, а ещё относится к анаэробному дыханию. Это процесс, в котором именно нитраты и продукты реакций восстановления нитратов, а не кислород, используются для окислительных реакций, и одни бактерии тем самым осуществляют окисление органических веществ, а другие окисляют минеральные вещества; при такого рода окислении выделяется энергия, и это часть метаболических процессов микроорганизмов.
В осуществлении денитрификации участвуют ферменты наподобие нитратредуктазы, редуктазы окиси и закиси азота. Полный процесс реакции с получением энергии под силу лишь прокариотам, способным как к обычному кислородному дыханию, так и к анаэробному, у эукариотов такое невозможно. Отдельные микроорганизмы проводят процесс не полностью, поскольку обладают лишь частью ферментов.
А есть такие микроорганизмы способны не только к денитрфикации, но и к азотфиксации. Эукариоты при денитрифкации не получают энергию, но они проводят этот процесс с целью очистить организм (как свой, так и окружающий «большой» организм, если речь идёт о клетках печени) от нитритов.
Как составить уравнение химической реакции: пошаговая инструкция

Превращение одних веществ в другие — обычное явление, которое происходит в ходе химических реакций. Для того чтобы обозначить, как протекают такие процессы, используют специальную систему уравнений. Так, например, горение метана (мы можем наблюдать его каждый день, когда зажигаем газовую плиту) протекает по следующей схеме:
СН4 + 2О2 → СО2 + Н2О
Расшифровать уравнение реакции можно следующим образом. Две молекулы кислорода соединяются с молекулой метана и в результате формируют две молекулы воды и молекулу углекислого газа. Можно отметить, что во время протекания реакции связи между некоторыми атомами (например, водорода и углерода) разрываются. Вместо них появляются новые, благодаря которым и формируются углекислород и вода.
Этапы разложения органики
Стадии разложения органических веществ бактериями гниения с химической точки зрения довольно сложны. В целом этот процесс осуществляется следующим образом:
- Метаболизм бактерий (ферментативная составляющая) основан на их возможности разорвать связи в молекулах азотсодержащих органических соединений. В процессе своего питания они захватывают белки и аминокислоты.
- В конечном итоге при воздействии ферментов-протеаз, в процессе гидролиза они разлагают их до простых неорганических веществ.
- Продукты. Полученные в результате этих химических реакций идут на постройку собственного организма и используются для накопления энергии в виде аденозинтрифосфорной кислоты (АТФ).
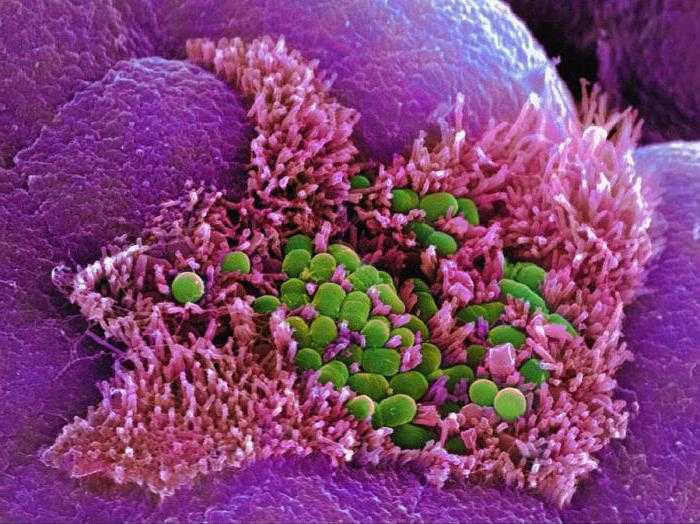
Какие вещества образуются
В первую очередь это конечные продукты: аммиак и сероводород. Также при неполной минерализации образуются:
- трупные яды (кадаверин, например);
- соединения ароматического характера (скатол, индол);
- при гниении аминокислот, содержащих серу, образуются тиолы, диметилсульфоксид.
Вообще-то, в рамках, контролируемых иммунитетом, процесс разложения – часть пищеварительного процесса для многих животных и для человека. Он происходит, как правило, в толстом кишечнике, и бактерии, вызывающие гниение, играют в нем первостепенную роль. Но в больших масштабах отравление продуктами гниения может привести к плачевным результатам. Человек нуждается в срочной медицинской помощи, промывании кишечника и восстанавливающей микрофлору терапии.
К тому же накопление в организме аммиака может инициироваться некоторыми видами бактерий, в том числе и кишечной палочкой. В результате в некоторых тканях накапливается аммиак. Но при нормальном функционировании всех систем он связывается до мочевины и затем выводится из организма человека.
Что такое гниение?
Гниение – это разложение белковых соединений, которые входят в состав растительных и животных организмов. В процессе из сложных органических веществ образуются минеральные соединения:
- сероводород;
- углекислый газ;
- аммиак;
- метан;
- вода.
Гниение всегда сопровождается неприятным запахом. Чем интенсивнее «душок», тем дальше зашел процесс разложения. Чего стоит «аромат», который издают останки дохлой кошки в дальнем углу двора.
Важным фактором для развития микроорганизмов в природе является тип питания. Гнилостные бактерии питаются готовыми органическими веществами, поэтому их называют гетеротрофы.
Самая благоприятная температура для гниения колеблется в пределах 25-35°C. Если температурную планку снизить до 4-6°C, то жизнедеятельность гнилостных бактерий можно значительно, но не полностью, приостановить. Вызвать гибель микроорганизмов способно только повышение температуры в пределах 100°C.
А вот при очень низких температурах гниение полностью останавливается. Ученые не раз находили в насквозь промерзшей земле Крайнего Севера тела древних людей и мамонтов, которые замечательно сохранились, несмотря на прошедшие тысячелетия.
2. Этапы гниения
Первой стадией разложения белков является их гидролиз как микробными протеазами, так и протеазами клеток погибшего организма, высвобождаемыми из лизосом в результате смерти клеток (аутолиз). Протеолиз происходит в несколько стадий- в начале белки расщепляются до всё ещё крупных полипептидов, затем образовавшиеся полипептиды расщепляются до олигопептидов, которые в свою очередь расщепляются до дипептидов и свободных аминокислот. Образовавшиеся свободные аминокислоты затем подвергаются ряду превращений, приводящих к выделению характерных для гниения продуктов. Первыми стадиями является дезаминирование аминокислот, в результате которого аминогруппа аминокислоты отщепляется и высвобождается свободный ион аммония и декарбоксилирование, в результате которого карбоксильная группа отщепляется с высвобождением двуокиси углерода (реакция декарбоксилирования чаще всего происходит в условиях пониженного pH). В результате декарбоксилирования высвобождаются также первичные амины:
H2N-(CH2)4-CHNH2-COOH (лизин) → H2N-(CH2)4-CH2NH2 (кадаверин) + CO2
Выделяют так называемое окислительное дезаминирование (наиболее распространённый вид дезаминирования, в результате которого NAD(P) восстанавливается до NAD(P)H2) и гидролитическое дезаминирование, при котором аминогруппа аминокислоты заменяется на гидроксильную.
Также некоторые аминокислоты трансаминируются путём перемещения аминогруппы аминокислоты на 2-оксикислоту (в результате этого процесса также происходит дезаминирование аминокислот, кроме этого синтезируются те аминокислоты, которые бактерии не могут синтезировать путём аминирования ионами аммония).
Образовавшиеся в результате дезаминирования и декарбоксилирования продукты могут как окисляться микроорганизмами с целью получения энергии в виде АТФ, так и участвовать в реакциях промежуточного обмена.
Что разлагается
Процессы разложения – это весь спектр реакций, в результате которых сложные вещества разлагаются до простых и более стойких. Процессом гниения (аммонификацией) называют разложение до простых молекул органических веществ, содержащих азот и серу. Сходный процесс – брожение – это разложение безазотистых органических веществ – сахаров или углеводов. И тот и другой процессы осуществляют микроорганизмы. Выяснение механизма данных процессов началось с опытов Луи Пастера (1822-1895). Если же посмотреть на бактерии гниения исключительно с химической точки зрения, то мы увидим, что причинами этих процессов является нестойкость органических соединений и микроорганизмы выступают лишь как возбудители химических реакций. Но и белок, и кровь, и животные под воздействием бактерий подвергаются разным типам гниения, то главенствующая роль именно микроорганизмов неоспорима.
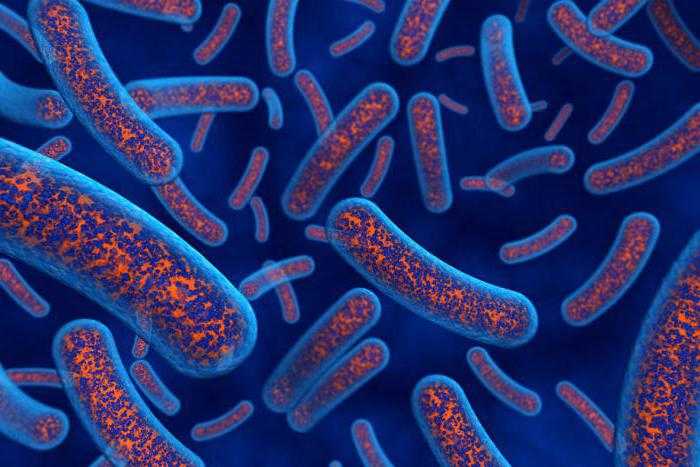
Образование скатола и индола
Анаэробное разложение белков представителями рода Clostridium
Характерной особенностью так называемых протеолитических клостридиев (то есть разрушающих белки — например Clostridium hystoliticum) является способность сбраживать аминокислоты (таким образом используя их для получения энергии и как источник углерода) и продуцировать протеолитические ферменты. Представители рода Clostridium способны сбраживать глутаминовую кислоту, глутамин, гистидин, лизин, аргинин, фенилаланин, серин, треонин, аланин и цистеин. Некоторые аминокислоты могут сбраживаться одиночно (например лизин, в результате сбраживания которого происходит образование аммиака, масляной и уксусной кислот), а некоторые лишь парами (при котором происходит сопряжённая окислительно-восстановительная реакция, в которой одна аминокислота выступает в роли донора электронов, а вторая- акцептора). Донорами электронов в реакциях парного сбраживания могут выступать аспарагин, аланин, валин, серин, гистидин, в роли акцептора — глицин, пролин, орнитин, аргинин.
Хорошо изучено сопряжённое окисление-восстановление пары аланина и глицина. Суммарно реакция выглядит так:
В результате парного сбраживания аланина и глицина бактерия получает 1 молекулу АТФ на каждую молекулу аланина.
Влияние человека на круговорот азота в природе
В последние столетия влияние человеческой деятельности на естественную циркуляцию азота в природе стало весьма ощутимым. Промышленная деятельность, загрязняющая воздух кислотными веществами, в числе которых есть и оксиды азота, приводит к кислотным дождям ‒ осадкам и снегу с пониженным pH (водородным показателем). Оксид азота создаётся в результате высоких температур, при которых осуществляется химическая реакция с соединением азота и кислорода (который составляет лишь 20 процентов воздуха).
На промышленных предприятиях, в том числе на тех, где сжигается органическое топливо, такие высокие температуры, подходящие для создания оксида азота, возникают в двигателях внутреннего сгорания и котлах. В естественных условиях оксид азота образуется во время грозы, при разрядах молний. Из-за антропогенной деятельности количество выделяемого оксида азота (II) увеличилось сверх естественной нормы, а оксид азот (II) может достаточно легко перейти в оксид азота (IV), после чего так же легко вступает в контакт с атмосферной влагой, и результатом становится формирование азотной и азотистой кислот, и эти кислоты во время осадков оказываются в почве, делая её менее благоприятной для жизнедеятельности, к примеру, растений.
Негативным последствием человеческой деятельности являются выбросы в атмосферу оксидов азота вследствие активного промышленного производства аммиака, азотной и серной кислот. Именно оксиды азота являются одним из наиболее распространённых загрязняющих веществ. Также активно изготавливают нитриты, нитратную селитру, органические удобрения, предназначенные для полевых, огородных и садовых работ, и чрезмерное насыщение почв этими веществами пагубно влияет на минеральный состав почвы, делая её менее плодородной.
Ещё одним примером отрицательного воздействия на азотистый почвенный обмен являются сточные воды, неконтролируемый выгул собак, свалки бытовых отходов, изношенная канализация ‒ иными словами, биологическое загрязнение почвы.
Результатом такого становится то, что в почве оказывается слишком много аммиака и солей аммония, меркаптанов и индола, других продуктов гниения органических веществ. Излишки аммиака под действием бактерий переходят в излишки нитратов, которые накапливаются в почве, отражаясь на её плодородности.
План:
- Введение
- 1 Аммонифицирующие микроорганизмы
-
2 Этапы гниения
2.1 Образование промежуточных и конечных веществ при гниении
- 3 образование метана
- 4 образование сероводорода
- 5 образование углекислого газа
- 6 образование меркаптанов
- 7 образование фосфина
- 8 образование водорода
- 9 образование оксикислот
- 10 образование жирных кислот
- 11 образование кетокислот
- 12 образование альдегидов
- 13 образование спиртов
- 14 образование сероуглерода
- 15 образование фенола и крезола
- 16 образование аммиака
-
17 образование скатола и индола
- 17.1 Распад нуклеиновых кислот
- 17.2 Распад аминов
- 17.3 Изменения жиров
- 17.4 Анаэробное разложение белков представителями рода Clostridium
- 18 Анаэробная и гнилостная инфекция
- 19 Судебная медицина
Примечания
Сенная палочка
Самая изученная бактерия — Bacillus subtilis, очень эффективный аммонификатор. Лучше нее изучена только кишечная палочка (Escherichia coli), наш кишечный симбионт. Сенная палочка — это аэробная бактерия гниения. На ее поверхности находятся ферменты-катализаторы протеазы, выработанные бактерией и используемые для получения жизненной энергии. Протеазы вступают в реакции гидролиза с белками внешней среды и разрушают его пептидные вязи с высвобождением начала крупных цепочек аминокислот, а потом все более мелких. Все, что ей необходимо, поступает в клетку, а что не нужно, отдается. И остаются токсичные вещества – сероводород и аммиак. Именно из-за этих газов места обитания сенных палочек так неприятно пахнут.
Аммиак в судебно-медицинском отношении
Аммиак может вызывать отравление в газообразном состоянии или при приемах внутрь в виде водных растворов. Клиническая картина при отравлении аммиаком (per os) сходна с той, которая наблюдается при отравлении едкими веществами, однако имеются особенности: характерен запах рвотных масс, насморк, слезотечение, сильный кашель; наблюдается парез нижних конечностей
При судебно-медицинском исследовании обращают внимание на ярко-красный цвет слизистой оболочки рта, глотки, пищевода и желудка, иногда принимающий более темную окраску. В легких наблюдается очаговая пневмония, в почках — явления острого нефрита.
При вскрытии трупа ощущается запах Аммиака, сохраняющийся в течение нескольких дней. Для судебно-химического качественного обнаружения аммиака используется способность его паров окрашивать в синий цвет красную лакмусовую бумажку и бумажку, смоченную раствором сульфата меди. Для исключения Аммиака, образующегося при гниении биол. объектов, параллельно проводится испытание с бумажкой, пропитанной раствором ацетата свинца. При этом возникает почернение в присутствии сероводорода, сопутствующего Аммиака при гниении. При посинении двух первых бумажек и потемнении третьей установление наличия поступившего в организм Аммиака химическим методом уже невозможно.
Количественное определение Аммиака при исследовании трупного материала, как правило, не может быть произведено.
Значение процесса гниения
Общебиологическое значение процесса гниения огромно. Гнилостные микроорганизмы являются «санитарами земли». Вызывая минерализацию громадного количества белковых веществ, попадающих в почву, осуществляя разложение трупов животных и растительных отбросов, они производят биологическую очистку земли. Глубокое расщепление белков вызывают споровые аэробы, менее глубокое — споровые анаэробы. В природных условиях этот процесс совершается поэтапно в содружестве многих видов микроорганизмов.
Но в пищевом производстве гниение является вредным процессом и наносит большой материальный ущерб. Порча мяса, рыбы, овощей, яиц, фруктов и других продуктов питания наступает быстро и протекает очень энергично, если хранить их незащищенными, в условиях, благоприятных для развития микробов.
Лишь в отдельных случаях в пищевом производстве гниение может быть использовано как полезный процесс — при созревании соленой сельди и сыров. Используется гниение в кожевенном производстве для швицевания шкур (удаление шерсти со шкур животных при выработке кож). Зная причины процессов гниения, люди научились защищать пищевые продукты белкового происхождения от их распада путем применения самых разнообразных методов консервирования.
Применение аммиака в медицине
Раздражающее действие аммиака и его солей используется в мед. практике. Рефлексы, возникающие при раздражении слизистых оболочек верхних дыхательных путей, способствуют возбуждению дыхательного центра, особенно при его угнетении (удушение, отравление и так далее). Вдыхание Аммиака вызывает учащение дыхания и повышение артериального давления; при действии больших концентраций, наоборот, происходит остановка дыхания и замедление пульса. Кроме того, при продолжительном действии высоких концентраций аммиака на месте применения его могут возникать воспалительные и некробиотические изменения в тканях. Аммиак обладает также дезинфицирующим действием.
Из препаратов аммиака наибольшее терапевтическое применение имеет нашатырный спирт (Solutio Ammonii caustici, Liquor Ammonii caustici, Ammonium causticum solutum, NH4OH) — 10% водный раствор Аммиака Прозрачная бесцветная жидкость с резким запахом аммиака. Смешивается с водой и спиртом в любых соотношениях. Нашатырный спирт вызывает раздражение рецепторов слизистых оболочек и рефлекторно возбуждает дыхательный и сосуд одвигательный центры. С этим свойством связано его применение при обморочных состояниях или отравлении алкоголем (ингаляция или прием внутрь по 5—10 капель в 100 мл воды). Действие на дыхательный центр непродолжительно, и для длительной стимуляции дыхания необходимо применение аналептиков. В хирургической практике нашатырный спирт применяют как дезинфицирующее средство для мытья рук (25 мл на 5 л теплой воды — способ Кочергина—Спасокукоцкого).
При хронических артритах и невралгиях в качестве отвлекающего средства применяют аммиачный линимент (Linimentum ammoniatum, линимент летучий, Linimentum volatile) — однородная густоватая жидкость желтовато-белого цвета с запахом аммиака. Получают взбалтыванием смеси подсолнечного масла (74 части) и олеиновой кислоты (1 часть) с раствором аммиака (25 частей).
Раствор аммиака при приеме внутрь оказывает отхаркивающий эффект (см. Нашатырно-анисовые капли).
Растворы Аммиака применяют для нейтрализации кислых токсинов при укусах насекомых, змей и каракурта (примочки или впрыскивания в место укуса). Имеются данные об использовании слабых растворов аммиака (0,1—0,2%) в качестве противовоспалительного средства при панарициях, фурункулах, абсцессах и тому подобное.
Такие простые и такие сложные
По форме бактерии могут быть шаровидные (кокки), прямые палочки (бациллы), выгнутые (вибрионы), спиральные (спириллы). Они могут объединяться – диплококки (два кокка), стрептококки (цепочка кокков), стафилококки (гроздь кокков). Клеточная стенка из муреина (полисахарида в соединении аминокислотами) придает форму организму и защищает содержимое клетки. Мембрана клетки из фосфолипидов может впячиваться и одержит комплексы органов движения (жгутиков). В клетках нет ядра, а в цитоплазме находятся рибосомы и кольцевая ДНК (плазмид). Органелл нет, а функции митохондрий, хлоропластов выполняют мезосомы – выпячивания мембраны. У некоторых имеются вакуоли: газовые выполняют функцию перемещения в толще воды, а в запасающих находятся гликоген или крахмал, жиры, полифосфаты.
18. Анаэробная и гнилостная инфекция
Анаэробная инфекция — тяжелая токсическая раневая инфекция, вызванная анаэробной гнилостной микрофлорой, с преимущественным поражением соединительной и мышечной ткани.
В хирургии принято выделять:
- Анаэробная клостридиальная(классическая) инфекция(гангрена газовая)
- Анаэробная неклостридиальная инфекция
- Гнилостная инфекция
При анаэробной инфекции(газовой гангрене) ткани, омертвевшие под действием экзотоксинов, образуемых бактериями рода Clostridium, колонизируются вторичной гнилостной микрофлорой.
Возбудителями анаэробной неклостридиальной инфекции являются представители нормальной микрофлоры человека, находящейся на коже, в полости рта, желудочно-кишечного тракта. Это бактероиды, пептококки, пептострептококки, актиномицеты, микрококки.
Гнилостная инфекция — инициируется представителями анаэробной неклостридиальной микрофлоры в сочетании с аэробными микроорганизмами (чаще стафилококками или граммотрицательными палочками Pseudomonas aeruginosa, Escherichia coli, Proteus vulgaris, Enterobacter aerogenes, Klebsiella)
Изучение предмета продолжается
Гниение имеет огромное значение как в экономии природы, так и в человеческой деятельности: от технических производств до развития болезней. Прикладная бактериология родилась всего порядка 50 лет назад, трудности изучения и сегодня громадны. Но перспективы огромны:
- Гниение и брожение активно используется в различных производствах – разделение растительных веществ, растительных волокон и стебля, зерен от мякоти и многое другое. Изучение процессов и микроорганизмов сулит новые технологии.
- Удаление органики необходимо при придании прочности растительным материалам (бумаги, древесины, ткани). И новые технологии этих производств уже в пути.
- Бактерии незаменимы в технологиях генной инженерии и производстве биологических лекарств. а их способности захватывать и выводить болезнетворные организмы сулит прорыв в медицине.
Источники аммиака в воде
Вы можете ощутить аммиак в воде на уровне около 35 ppm. Более низкие уровни аммиака естественным образом проявляются в пищевых продуктах и воде. Проглатывание даже небольшого количества жидкого аммиака в чистящей жидкости может привести к ожогам во рту и горле. Несколько капель жидкого аммиака на коже или в глазах могут вызвать ожоги и открытые язвы, если их быстро не смыть. Воздействие больших количеств жидкого аммиака или ионов аммония в глазах вызывает сильные ожоги глаз и может привести к слепоте.
Бытовые и промышленные растворы для уборки могут содержать аммиак, и использование этих средств дома или на работе может привести к воздействию аммиака. Оба вида растворов для уборки аммиака производятся путем добавления в воду газа аммиака для образования жидкого аммиака.
Средства для очистки помещений обычно содержат более низкие уровни аммиака (от 5 до 10%) по сравнению с промышленными растворами для очистки, которые могут содержать более высокие уровни аммиака (до 25%).
Что такое гниение
Суть в том, что сложнейшая по своему составу материя распадается на более простые элементы. Современное представление ученых об этом процессе, превращающем органические соединения в неорганические, можно описать следующими действиями:
- Бактерии гниения обладают метаболизмом, что разрывает химическим путем связи молекул органики, содержащих азот. Процесс питания происходит в форме захвата молекул белка и аминокислот.
- Ферменты, что выработаны микроорганизмами, в процессе расщепления высвобождают аммиак, амины, сероводород из молекул белка.
- Продукты, поступающие в организм бактерии гниения, используются для получения энергии.



















![Круговорот азота [1969 германов н.и. - микробиология]](http://zd-semya.ru/wp-content/uploads/6/9/c/69ca61cfd0d31e566b2277788e86048d.jpeg)














